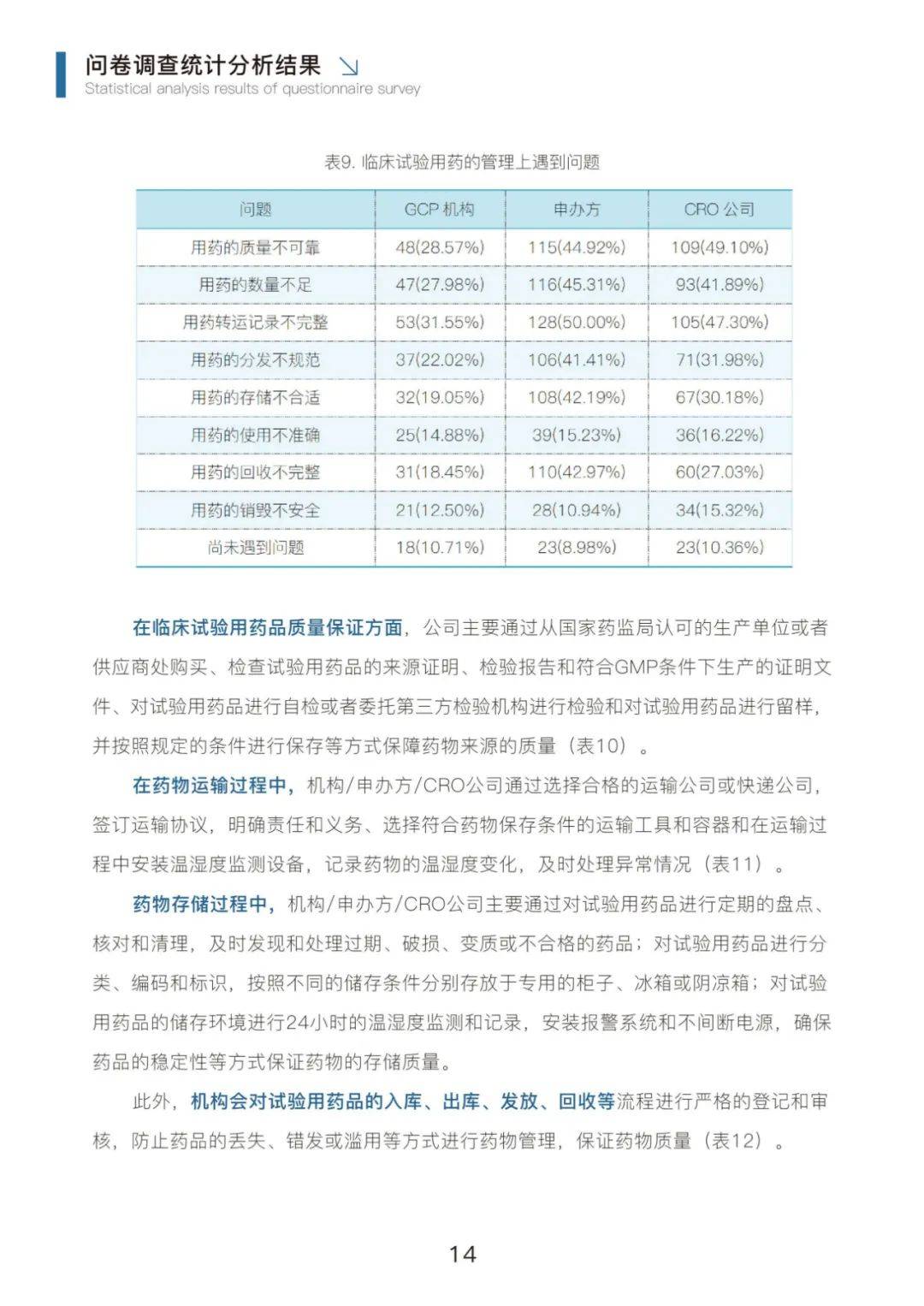
在临床试验用药品质量保证方面,公司主要通过从国家药监局认可的生产单位或者供应商处购买、检查试验用药品的来源证明、检验报告和符合GMP条件下生产的证明文件、对试验用药品进行自检或者委托第三方检验机构进行检验和对试验用药品进行留样并按照规定的条件进行保存等方式保障药物来源的质量(表10)。
在药物运输过程中,机构/申办方/CRO公司通过选择合格的运输公司或快递公司,签订运输协议,明确责任和义务、选择符合药物保存条件的运输工具和容器和在运输过程中安装温湿度监测设备,记录药物的温湿度变化,及时处理异常情况。
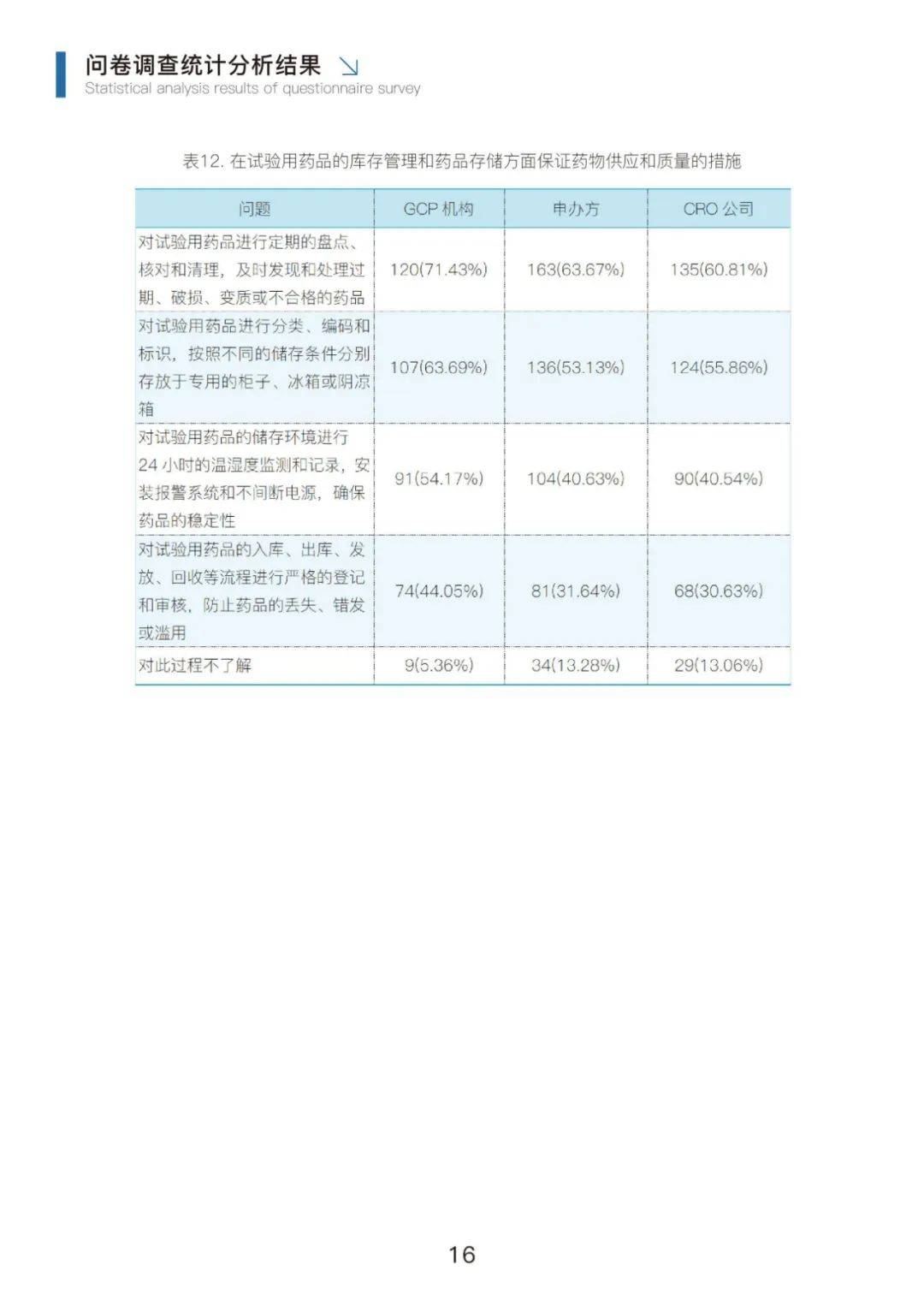
药物存储过程中,机构/申办方/CRO公司主要通过对试验用药品进行定期的盘点核对和清理,及时发现和处理过期、破损、变质或不合格的药品;对试验用药品进行分类、编码和标识,按照不同的储存条件分别存放于专用的柜子、冰箱或阴凉箱;对试验用药品的储存环境进行24小时的温湿度监测和记录,安装报警系统和不间断电源,确保药品的稳定性等方式保证药物的存储质量。
此外,机构会对试验用药品的入库、出库、发放、回收等流程进行严格的登记和审核,防止药品的丢失、错发或滥用等方式进行药物管理,保证药物质量。








声明:本站所有文章,如无特殊说明或标注,均为本站原创发布。任何个人或组织,在未征得本站同意时,禁止复制、盗用、采集、发布本站内容到任何网站、书籍等各类媒体平台。如若本站内容侵犯了原著者的合法权益,可联系我们进行处理。

